
El 7 de noviembre, la Administración de Alimentos y Medicamentos de los Estados Unidos (FDA) emitió un aviso en su sitio web oficial, anunciando que después de una rigurosa revisión científica, ha otorgado a Swedish Match USA, Inc. una extensión para la autorización de riesgo modificado para ocho variedades de productos de snus. Con esta extensión, estos productos pueden seguir siendo vendidos (ya se les permitió ser vendidos desde 2019) y vienen con la siguiente declaración de riesgo modificado: "Usar snus en lugar de cigarrillos puede reducir el riesgo de cáncer oral, enfermedades cardíacas, cáncer de pulmón, accidente cerebrovascular, enfisema y bronquitis crónica.
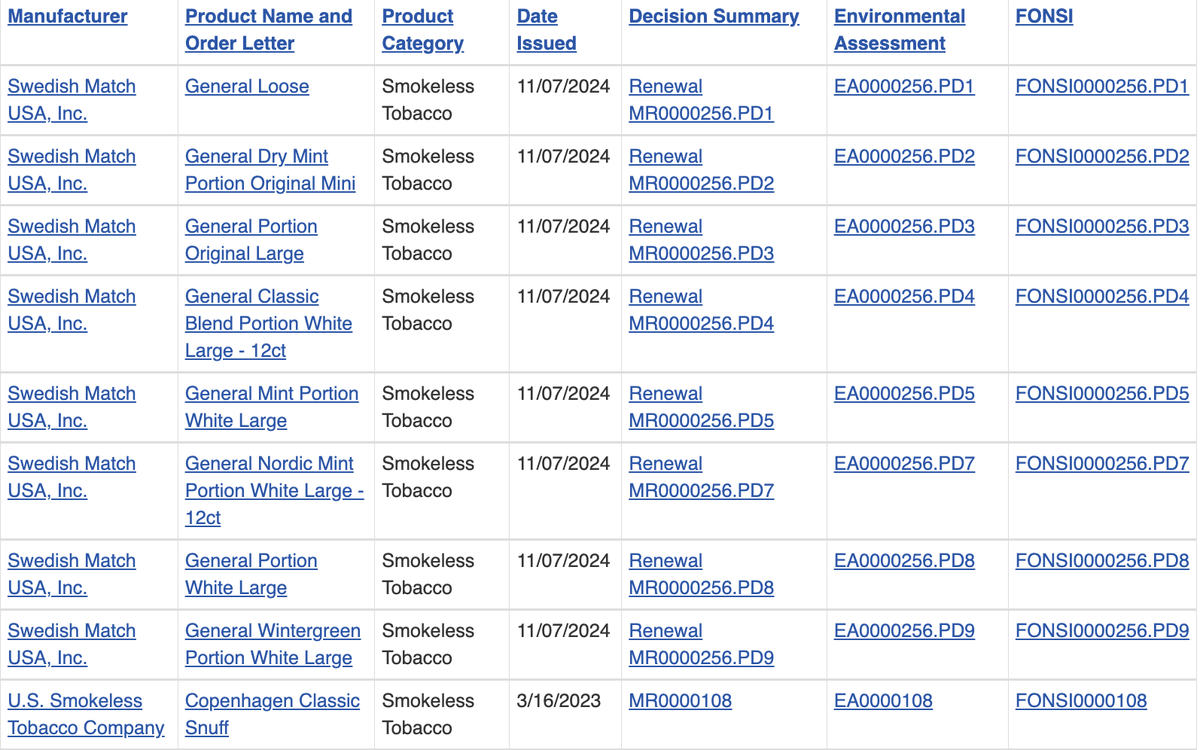
Productos que han recibido órdenes de corrección de riesgos incluyen:
General Suelto General Menta Seca Original Mini General Porción Original Grande General Mezcla Clásica Porción Blanca Grande-12 unidades General Menta Porción Blanca Grande General Menta Nórdica Porción Blanca Grande-12 unidades General Porción Blanca Grande General Invierno Porción Blanca Grande.
La FDA ha emitido una orden de corrección de riesgos que específicamente apunta a los productos mencionados anteriormente, efectiva hasta el 7 de noviembre de 2032. Si en cualquier momento la agencia determina que seguir vendiendo estos productos ya no es beneficioso para la salud general de la población, la agencia puede revocar la orden.
La FDA declaró que, luego de revisar la evidencia, hay un respaldo científico para afirmar que estas declaraciones de reducción de riesgos pueden ayudar a los consumidores a comprender los riesgos relativos de estos productos en comparación con los cigarrillos. La FDA encontró que estos productos de reducción de riesgos, cuando son utilizados por los consumidores, reducirán significativamente el daño a los usuarios de tabaco y el riesgo de enfermedades relacionadas con el tabaco, beneficiando la salud de la población en general. En particular, la evidencia científica existente, incluidos estudios epidemiológicos a largo plazo, muestra que el uso exclusivo de estos productos puede disminuir el riesgo de cáncer oral, enfermedades cardíacas, cáncer de pulmón, accidente cerebrovascular, enfisema y bronquitis crónica en comparación con fumar. La evidencia existente no indica que un gran número de jóvenes esté comenzando a utilizar estos productos.
La FDA enfatiza específicamente que la orden de riesgo modificado no permite a la empresa comercializar el producto con ninguna otra declaración de riesgo modificada que pueda transmitir o confundir a los consumidores haciéndoles creer que el producto está aprobado o respaldado por la FDA, o que la FDA ha considerado el producto seguro para los consumidores. No existe un producto de tabaco seguro, y las personas que no usan productos de tabaco no deberían comenzar a hacerlo.
La FDA señaló que esta es la primera vez que la FDA ha renovado y modificado una orden de aprobación de riesgos.
Estos productos fueron inicialmente aprobados para un descargo de responsabilidad de enlace externo en 2015, y fueron comercializados en Estados Unidos a través del proceso de solicitud de productos de tabaco pre-mercado. En octubre de 2019, el producto fue autorizado para la venta como un producto de tabaco de riesgo modificado con un descargo de responsabilidad de enlace externo. La orden que permite la venta de productos de snus como productos de tabaco de riesgo modificado en 2019 es válida por 5 años. Para poder seguir vendiendo estos productos después de la fecha límite especificada en la orden de 2019, Swedish Match ha presentado una solicitud de renovación para productos de tabaco de riesgo modificado.
Aviso
1.Este artículo se proporciona exclusivamente para fines de investigación profesional relacionados con la industria, la tecnología y la política. Cualquier referencia a marcas o productos se realiza únicamente con fines descriptivos y no constituye un respaldo, recomendación o promoción de ninguna marca o producto.
2.El uso de productos de nicotina, incluidos pero no limitados a cigarrillos, cigarrillos electrónicos y productos de tabaco calentado, está asociado con riesgos significativos para la salud. Se requiere que los usuarios cumplan con todas las leyes y regulaciones pertinentes en sus respectivas jurisdicciones.
3.El acceso o la visualización de este artículo está estrictamente prohibido para personas que no hayan alcanzado la edad legal.
Aviso de Derechos de Autor
Este artículo es una obra original de 2Firsts o una reproducción de fuentes de terceros con la fuente original claramente indicada. Los derechos de autor y los derechos de uso de este artículo pertenecen a 2Firsts o a la fuente original. La reproducción, distribución o cualquier otro uso no autorizado de este artículo por cualquier entidad o individuo está estrictamente prohibido. Los infractores serán legalmente responsables. Para asuntos relacionados con los derechos de autor, por favor contacte a: info@2firsts.com
Descargo de Responsabilidad por Asistencia de IA
Este artículo puede haber utilizado IA para mejorar la eficiencia en la traducción y edición. Sin embargo, debido a limitaciones técnicas, pueden ocurrir errores. Se recomienda a los lectores que consulten las fuentes proporcionadas para obtener información más precisa.
Este artículo no debe utilizarse como base para decisiones o consejos de inversión, y 2Firsts no asume ninguna responsabilidad directa o indirecta por cualquier error en el contenido.

