La partida del director de la Oficina de Ciencias del Tabaco de la Administración de Alimentos y Medicamentos de Estados Unidos de la industria tabacalera pone de relieve un problema de larga data conocido como "puerta giratoria" entre las agencias regulatorias gubernamentales y las industrias que supervisan.
El martes, Matt Holman dejó la FDA para trabajar en Philip Morris International, una compañía que vende productos como los cigarrillos Marlboro y el dispositivo electrónico de tabaco IQOS en el extranjero. El trabajo de Holman en la FDA tuvo un impacto en las decisiones relacionadas con la seguridad de productos como los cigarrillos electrónicos.
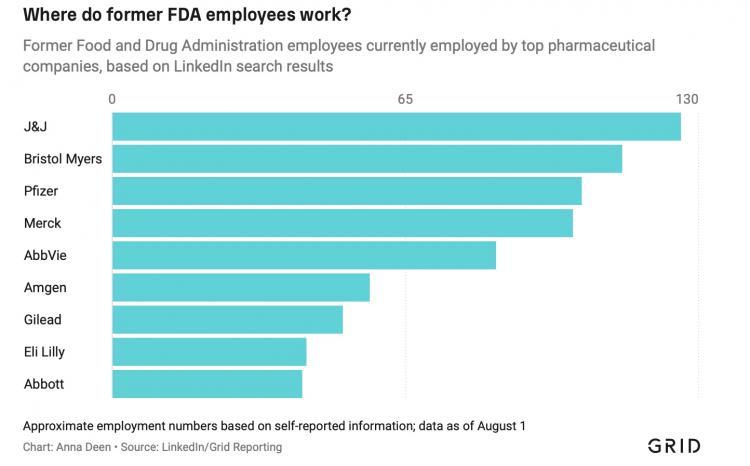
Las agencias de supervisión regulatoria afirman que donde hay humo, hay fuego de moralidad. Durante décadas, han estado advirtiendo sobre el problema de la puerta giratoria, que solo ha sido bien documentado en puestos de alto nivel y dentro del Departamento de Defensa. Sin embargo, los datos concretos sobre la magnitud del problema han sido escasos. Un análisis de datos personales de LinkedIn muestra que al menos 2,700 ex empleados de la FDA están trabajando actualmente en la industria farmacéutica. Según la información de los perfiles personales, otros 1,100 empleados actuales de la FDA han hecho la transición desde la industria hacia la agencia.
Antiguos empleados de la FDA también pueden encontrarse en muchos otros sectores que la agencia regula: alrededor de 1.200 trabajan actualmente en biotecnología y más de 600 trabajan en dispositivos médicos. Algunos ejemplos destacados incluyen a Scott Gottlieb, ex director de la FDA durante la administración Trump, quien se unió a la junta directiva de Pfizer pocas semanas después de dejar la agencia, y el actual comisionado Robert Califf, quien lideró la FDA durante la administración Obama antes de encabezar una subsidiaria de salud de Alphabet Inc. y regresar para liderar la agencia este año. Califf se comprometió a no trabajar para compañías farmacéuticas o de dispositivos médicos dentro de los cuatro años de dejar su posición actual después de ser confirmado por el Senado.
El recién nombrado director del Centro de Productos de Tabaco de la FDA, Brian King, anunció el 26 de julio que Matt Holman ha dejado su cargo relacionado con las decisiones regulatorias sobre el tabaco y ha tomado una licencia antes de julio. King expresó su agradecimiento por las contribuciones de Holman al centro a lo largo de los años y su compromiso inquebrantable.
Michael Carome, de la organización Public Citizen, que supervisa la salud pública en Washington D.C., comentó sobre estas cifras, afirmando que son interesantes y previsibles. Además, agregó que este número podría subestimar la cantidad de empleados que se trasladan a la industria que una vez regulaban, y no incluye a profesionales de la industria que permanecen brevemente en la agencia reguladora antes de regresar a su industria de origen, otra área de preocupación para los expertos en ética.
Walter Shaub, el experto en ética gubernamental a cargo de un proyecto de supervisión gubernamental, afirmó que "desafortunadamente, cuando se ve a alguien pasar de una agencia reguladora a una industria regulada, el público reacciona naturalmente con un sentimiento de traición, ya que esto plantea preguntas sobre su compromiso con la misión de proteger al público". Shaub mencionó que aunque las empresas reguladas pueden querer genuinamente ser responsables de supervisar el conocimiento profesional de su personal, "también quieren saber cómo opera la FDA en su interior".
Podrían estar pensando, o las personas podrían sospechar que están tratando de crear un ambiente donde los empleados de la FDA sepan que mientras no interrumpan verdaderamente a la industria regulada, puede haber un trabajo rentable esperándolos, ¿verdad? Simplemente creo que es la naturaleza humana", agregó.
Carome señaló que las preocupaciones sobre las puertas giratorias han fluctuado con las noticias sobre medidas como las tomadas por Holman. Durante la administración Trump, también hubo mucha preocupación ya que los funcionarios del gabinete y el propio presidente enfrentaron denuncias éticas relacionadas con sus lazos empresariales. Carome añadió: "Simplemente hay una falta de datos sobre la magnitud del problema a nivel del personal de la agencia".
Dorothy Norris-Tirrell, Directora de Aprendizaje de la Nonprofit Leadership Alliance, señaló que si bien el conjunto de datos de LinkedIn incluye información sobre 645 millones de personas y 56 millones de empresas, tiene limitaciones. Su propia investigación sobre trayectorias profesionales en el sector sin ánimo de lucro utilizó datos de LinkedIn, pero advirtió que los datos son autodeclarados y no se actualizan de manera constante. Sin embargo, Norris-Tirrell sugirió que los datos se pueden utilizar para identificar tendencias, como el movimiento de las personas de la FDA a otras industrias, sus cargos y su antigüedad en la agencia. También destacó que podría haber ideas interesantes obtenidas al segmentar los datos. Según los registros exhaustivos de LinkedIn, actualmente hay aproximadamente 16,000 personas empleadas en la FDA, lo que representa casi el 90% del personal a tiempo completo de la agencia.
En cuanto a Holman, Philip Morris International declaró en un comunicado de prensa enviado a Grid que el exfuncionario de la FDA está "dedicado a ayudar a los fumadores adultos actuales a acceder a alternativas libres de humo científicamente validadas, al mismo tiempo que protege a los jóvenes".
Holman ha sido prohibido de comunicarse con la FDA sobre Philip Morris y cualquier actividad en la que haya participado personalmente en la agencia durante un año, según las reglas éticas. Holman defendió sus acciones ante The New York Times, afirmando que consultó con el abogado de ética de la agencia y creía que si Philip Morris International estaba haciendo la transición de los cigarrillos a productos de tabaco menos perjudiciales, podría haber ingresado a la industria antes después de trabajar en la FDA durante 20 años. (No ha respondido a la solicitud de comentarios de Grid).
Sin embargo, según los datos de LinkedIn, muchos empleados de asuntos regulatorios o desarrollo de medicamentos en empresas farmacéuticas bajo la supervisión de la Administración de Alimentos y Medicamentos de Estados Unidos (FDA, por sus siglas en inglés), incluyendo a Merck, Abbott y Johnson & Johnson, trabajaron en la FDA durante más de una década antes de ingresar a la industria. Diana Zuckerman, presidenta del Centro Nacional de Investigación en Salud, dijo: "La idea de que están evitando conflictos es absurda porque le están diciendo a las empresas cómo manipular el sistema detrás de escena".
La partida de Hallman se produce en medio de los esfuerzos de la administración de Biden para regular la industria del tabaco, con planes para obligar a reducir los niveles de nicotina en los cigarrillos hasta hacerlos menos adictivos y comenzar a eliminar gradualmente los cigarrillos mentolados. Una ley de 2016 llevó a una represión contra los cigarrillos electrónicos, amenazando a las pequeñas tiendas de cigarrillos electrónicos y dando lugar a demandas contra Juul. El mes pasado, la agencia ordenó al fabricante de cigarrillos electrónicos que dejara de vender sus productos, a pesar de permitir que el gigante tabacalero RJR venda sus propios cigarrillos electrónicos. El plan de la agencia para regular el tabaco y la seguridad alimentaria está actualmente siendo revisado externamente debido a las recientes escaseces de fórmula infantil y al aumento de adolescentes que consumen nicotina desde 2017.
Stanton Glantz, crítico de larga trayectoria de la industria tabacalera y fundador del Centro de Investigación y Educación sobre Control del Tabaco en la Universidad de California, San Francisco, expresó que el Centro de Productos de Tabaco ha tomado muchas decisiones extrañas.
Al igual que otras compañías tabacaleras, Philip Morris International ha optado por el tabaco "no combustible" y dispositivos de cigarrillos electrónicos como parte de sus esfuerzos para superar las ventas de cigarrillos. El 11 de marzo, Holman firmó una "orden de riesgo modificado" de la FDA que autoriza a la compañía a utilizar lenguaje para comercializar sus productos de tabaco calentado, afirmando que estos productos "reducen significativamente la exposición a sustancias químicas dañinas o potencialmente dañinas".
of3gejhlgub462ohvhq9hhtqsza2rrtr
Shaub señaló que aunque las leyes federales de ética exigen que los exfuncionarios de la agencia eviten estrictamente los asuntos que ellos mismos hayan manejado, estas reglas no impiden que sus colegas o subordinados traten con ellos. Además de carecer de fuerza, la ley no tiene la capacidad de proteger contra un castigo más allá de la posibilidad de ser despedido, lo cual no representa una gran amenaza para aquellos que ya han dejado la institución. Si bien no es necesariamente práctico o aconsejable prohibir a cada empleado de la FDA que trabaje en la industria regulada, Shaub pidió fortalecer las reglas para aquellos que desempeñan los roles más críticos, específicamente aquellos que deciden permitir productos rentables, incluido el tabaco, que sigue siendo la principal causa evitable de muerte en América y que podría dañar al público.
La administración de Biden intentó abordar el fenómeno de la puerta giratoria el año pasado al ordenar a los nombrados que se comprometieran a no manejar asuntos relacionados con la agencia que supervisaban durante dos años después de dejar el cargo, y a no ayudar a otros en el cabildeo para obtener esas posiciones durante un año. La senadora Elizabeth Warren de Massachusetts, una demócrata, planteó preguntas sobre la contratación de funcionarios del Departamento del Tesoro y del Servicio de Impuestos Internos por parte de empresas de preparación de impuestos y copatrocinó la Ley de Anticorrupción y Integridad Pública durante la administración Trump con el objetivo de frenar el uso de la puerta giratoria por parte de altos funcionarios.
Declaración
Este artículo está elaborado a partir de información de terceros y está destinado únicamente para el intercambio y aprendizaje relacionados con la industria.
Este artículo no representa las opiniones de 2FIRSTS y 2FIRSTS no puede confirmar la autenticidad o precisión de su contenido. La traducción de este artículo es únicamente para el intercambio e investigación de la industria.
Debido a las limitaciones en la capacidad de traducción, el artículo traducido puede no expresar totalmente el mismo significado que el texto original. Por favor, consulte el texto original para obtener precisión.
2FIRSTS está completamente alineado con la postura del gobierno chino en cualquier declaración y posición relacionada con asuntos nacionales, Hong Kong, Macao, Taiwán y relaciones exteriores.
El derecho de autor de la información compilada pertenece al medio original y al autor. Si se produce alguna infracción, por favor contáctenos para su eliminación.
Este documento ha sido generado mediante traducción automática por inteligencia artificial y se proporciona únicamente con fines de discurso e aprendizaje de la industria. Ten en cuenta que los derechos de propiedad intelectual del contenido pertenecen a la fuente de medios original o al autor. Debido a ciertas limitaciones en el proceso de traducción, puede haber discrepancias entre el texto traducido y el contenido original. Recomendamos consultar la fuente original para obtener una precisión completa. En caso de inexactitudes, te invitamos a ponerte en contacto con nosotros para realizar correcciones. Si crees que algún contenido ha infringido tus derechos, por favor, ponte en contacto con nosotros de inmediato para su eliminación.


